En este artículo te contamos todo lo que necesitas saber sobre el aminoácido esencial L-Fenilalanina.
Índice
Qué es la L-fenilalanina
La L-fenilalanina es un aminoácido, es decir, un elemento constituyente de las proteínas.
A nivel funcional es un nutriente indispensable, ya que nuestro organismo no posee la capacidad de sintetizarlo de forma endógena. Es por esto por lo que requerimos de su consumo a través de la dieta u otra vía de administración externa para no sufrir caquexia.

Figura I. Representación gráfica de un proceso caquéxico.
Déficit de fenilalanina
Sufrir caquexia por una insuficiencia del aminoácido exclusivamente es prácticamente imposible y nunca ha sido reportado en la literatura científica salvo en casos de pacientes con nutrición parenteral.
La caquexia, y en general la malnutrición proteica, ocurre por consumos pobres del nutriente en general y no tanto de un aminoácido en sí mismo.
Sin embargo, la fenilalanina no solamente es esencial para la síntesis de proteínas, ya que en el organismo cumple una importante función endocrina en la síntesis de catecolaminas; y las características de su estructura química le otorgan una peculiaridad muy interesante frente a otros.
Dónde puedo encontrar fenilalanina
Está presente en prácticamente cualquier fuente de proteína:
- Carnes (ternera, aves de corral, cerdo).
- Pescados.
- Leche y derivados lácteos.
- Huevos.
- Productos de soja (en polvo, harinas y tofu).
- Ciertos frutos secos la poseen en pequeñas concentraciones.
Aspartamo y fenilalanina
Algo interesante es que una fuente es el aspartamo.
Obviamente, de forma significativa en sociedades desarrolladas e industriales (especialmente Estados Unidos, donde el consumo de aspartamo es muy alto). 
Figura II. Desglose de la estructura química del aspartamo, un dipéptido metil éster.
Aún así, un adulto medio ingiere aproximadamente 5g de L-fenilalanina al día cuando la ingesta dietética recomendada en base a una dieta isoenergética para un varón promedio es de 8g al día (HDMB, s.f.).
Por lo a pesar de su gran presencia de en alimentos de uso común, parece que nuestra ingesta no llega a ser suficiente acorde a las proporciones de establecidas.

Figura III. Recomendaciones de ingesta (g/kg/día) en función de la edad.
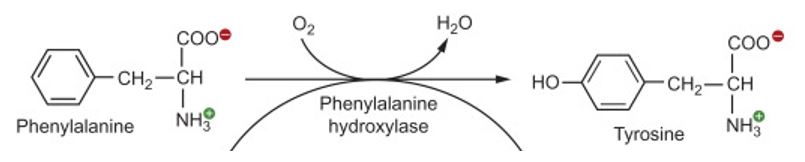
Figura IV. Representación gráfica del proceso de conversión (hidroxilación) de la L-fenilalanina a L-tirosina.
Para qué sirve la L-fenilalanina
Síntesis de proteínas musculares
Cualquiera de los aminoácidos proteinogénicos que codifican nuestro genoma puede, y será, utilizado para desarrollar los tejidos del organismo, incluyendo el tejido muscular.

Figura V. Representación gráfica de 20, de los actualmente propuestos 22, aminoácidos proteinogénicos.
De ellos, los aminoácidos esenciales son especialmente sensiblesen el proceso.
Aquí no hay tutía, o se administran de fuera o si mantenemos a largo plazo un consumo deficitario de alguno de ellos sufriremos un proceso catabólico para obtenerlos a partir de nuestras proteínas integrales.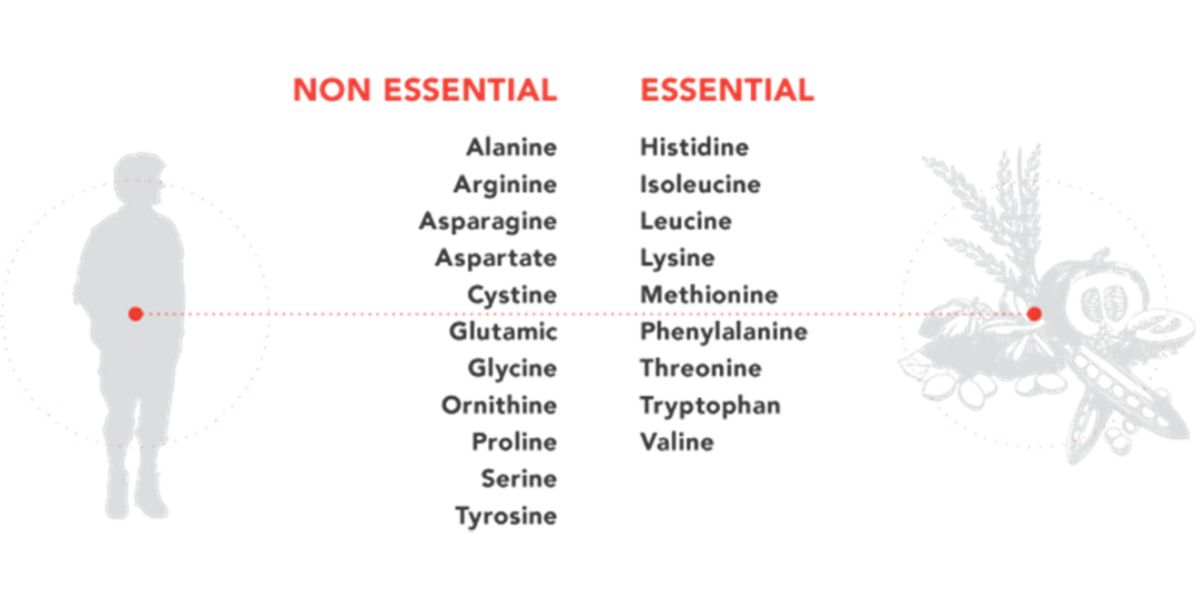
Figura VI. Representación gráfica de la categorización funcional en esenciales/no esenciales.
Es por esto por lo que asegurar el consumo de todos los aminoácidos esenciales es de suma prioridad y, teniendo en cuenta que un poco os he dejado la tabla de las cantidades recomendadas de estos, no estaría mal revisar vuestra dieta para ver si estáis bien cubiertos.
Síntesis de catecolaminas
La L-fenilalanina es el aminoácido que inicia el proceso de síntesis de catecolaminas.
Siendo estrictamente académicos, lo inicia la L-tirosina, pero como la fenilalanina se convierte en tirosina se puede decir que ésta es realmente el “primer paso funcional”. Este proceso ocurre en el hígado, a través de la acción de una enzima hidroxilasa.

Figura VII. Proceso de síntesis de las catecolaminas.
A partir de ahí, la tirosina se dirige a las neuronas dopaminérgicas y noradrenérgicas del sistema nervioso central, a los nervios simpáticos y a los feocromocitos de la médula adrenal y a los paraganglios en la periferia para sintetizar L-dopa, y esta a su vez continúa para generar dopamina y esta a su vez epinefrina y norepinefrina.
Todo el proceso tiene importantes implicaciones neurometabólicas, específicas a cada hormona que ha sido sintetizada, es decir, la dopamina tiene un rol en el sistema límbico y otras estructuras tanto corticales como extracorticales sobre la regulación de las emociones. 
Figura VIII. Representación gráfica simplificada del mecanismo de producción de la dopamina y la serotonina y sus efectos centrales.
Mientras que las funciones de la adrenalina y la noradrenalina están más caracterizadas por su perfil estimulante del sistema nervioso simpático, mediadas por los receptores adrenérgicos que modulan la contracción/relajación del músculo liso, incrementan la lipólisis, activan el sistema RAAs, etc. 
Figura IX. Principales efectos del agonismo a receptores alfa y beta adrenérgicos en diferentes tejidos.
Esta es la razón por la que la L-fenilalanina posee un papel sobre procesos como la lipólisis (primer paso de la “quema de grasas”); ya que a partir de ella, se sintetizan las hormonas responsables de este efecto.
La evidencia es un poco conflictiva, especialmente porque hay que tener en cuenta que la enzima limitante de la síntesis de catecolaminas es la tirosina hidroxilasa, y que al consumir un precursor, su actividad no se verá afectada.
Aun así, intervenciones como las de Ueda et al. (2017) muestran un aumento agudo de las concentraciones de glicerol en plasma, una muestra de hidrólisis de los triglicéridos intracelulares del lipid droplet de los adipocitos, y por tanto de lipólisis.

Regulación de la saciedad
Quizás la propiedad más curiosa y destacable de este aminoácido:
La fenilalanina es un nutriente altamente saciante.
Esto se debe a la influencia que posee sobre la secreción de colecistoquinina (CKK), una hormona peptídica que se produce en el duodeno y regula ciertos procesos de la digestión, entre ellos la regulación de la velocidad del vaciado gástrico.
Gracias a este efecto, la colecistoquinina ha sido propuesta como un potente supresor del apetito (Johnson, 2013); la auténtica hormona que antagoniza la acción de la ghrelina más que la leptina realmente por sus mecanismos.
La colecistoquinina se secreta ante alteraciones mecánicas del volumen gástrico, es decir, es la que nos da la sensación de saciedad cuando nos “llenamos” aunque sea de lechuga, comparte mecanismo con el PYY.
Además de esto, la secreción de colecistoquinina es tremendamente sensible a las concentraciones de ácidos grasos y aminoácidos presentes en el quimo a su paso por el intestino.

Los aromáticos (como la fenilalanina, la tirosina, o el triptófano) son los más efectivos para incrementar la secreción de CKK (Liddle, 1994), y entre todos ellos, la fenilalanina parece ser el más potente de todos aunque no conocemos con precisión sus mecanismos.
Ha demostrado modular las concentraciones intracelulares de calcio en los enterocitos de modelos animales, y lo que es más importante, en humanos ha demostrado ejercer un efecto anorexígeno.

Figura X. Efectos sobre el consumo calórico tras el consumo de L-fenilalanina (L-PA), D-fenilalanina (D-PA) y Placebo en una intervención ad libitum.
El grupo que consumió L-fenilalanina antes de la comida se sació mucho antes que el grupo que consumió D-fenilalanina o placebo y, por lo tanto, su ingesta energética fue mucho menor.
Este efecto se alcanzó gracias a los cambios en la secreción de CKK en el grupo L-fenilalanina, sin embargo, y contra la lógica, el grupo que usó D-fenilalanina no sufrió los mismos cambios.
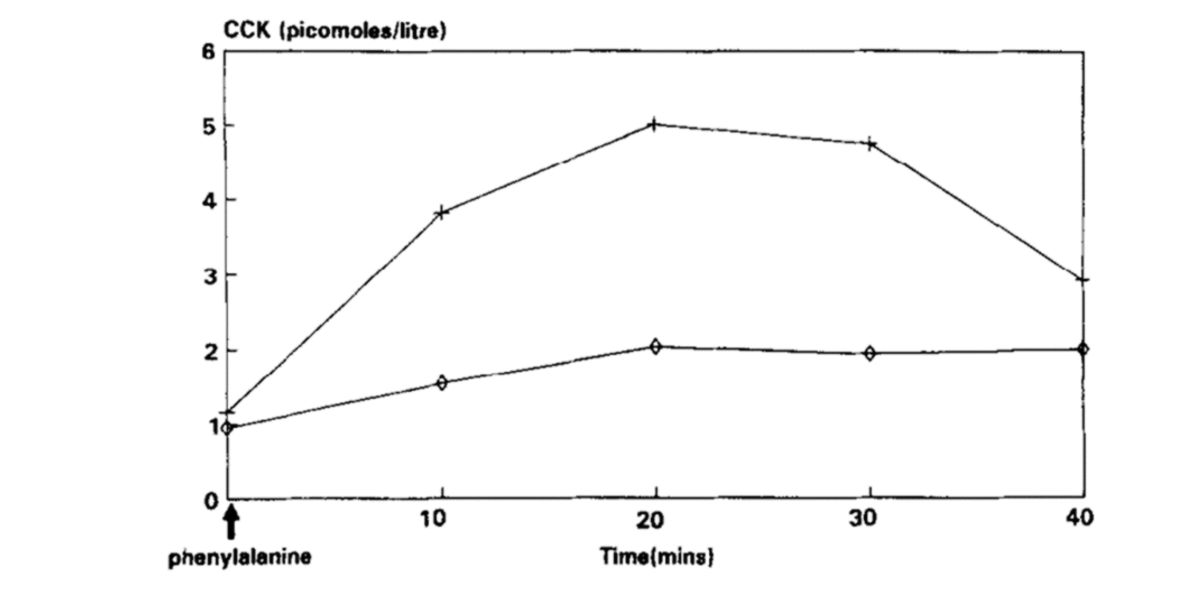
Figura XI. Curva de secreción de CKK tras la administración de L-fenilalanina (cruces) y D-fenilalanina (rombos).
Como ya sabemos desde hace años, la quiralidad y la configuración estereoisomérica de los aminoácidos que influye en su mecanismo de acción, farmacocinética y farmacodinamia.
L-Fenilalanina de HSN
En HSN hemos realizado un screening de la literatura científica sobre el uso de la L-fenilalanina y consideramos que es un nutriente que está suficientemente caracterizado y cuenta con una fuerte evidencia en humanos.
Siguiendo nuestra filosofía tradicional de la gama RawSeries, un producto de máxima pureza, sin aditivos que alteren el contenido del complemento alimenticio.
100% Vegan
En la lista de ingredientes de nuestra fenilalanina encontrarás: L-fenilalanina (producido a través de un proceso de fermentación vegetal). ¡Y nada más!
La denominación de “producido a través de un proceso de fermentación vegetal” se debe a nuestra creencia de que los suplementos nutricionales deben ser accesibles para todo el mundo independientemente de su condición o posición respecto al consumo de cualquier tipo de alimento.
Por eso encontrarás esto en nuestros productos:

Figura XII. “A destacar” en HSN, ausencia de alérgenos y aptitud en dietas vegetarianas y veganas.
Que indica:
Ausencia de alérgenos
Que siempre trabajamos para seleccionar materias primas de máxima calidad, y formular productos lo más libres posibles de estos compuestos.
Producto apto para vegetarianos y veganos
Desde hace meses rechazamos los aminoácidos derivados de fuentes animales, y ya únicamente utilizamos materias primas sin uso de los mismos, en su mayoría, procedentes de fuentes vegetales como el maíz.
¡Máxima pureza de origen vegetal! ¿Qué más necesitamos?
Fuentes Bibliográficas
- EFSA Panel on Dietetic Products, N. and A. (NDA). (2010). Scientific Opinion on the substantiation of health claims related to L phenylalanine and increased alertness (ID 708, 1629), enhancement of mood (ID 657), pain relief (ID 657) and improvement of memory (ID 658) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal, 8(10), 1748.
- Konturek, S. J., Radecki, T., Thor, P., & Dembinski, A. (1973). Release of Cholecystokinin by Amino Acids. Proceedings of the Society for Experimental Biology and Medicine, 143(2), 305–309.
- Matthews, D. E. (2007). An Overview of Phenylalanine and Tyrosine Kinetics in Humans. The Journal of Nutrition, 137(6), 1549S-1555S.
- National Center for Biotechnology Information. PubChem Database. Phenylalanine, CID=6140.
- National Center for Biotechnology Information. PubChem Database. Cholecystokinin, CID=16129670.
- Pacak, K., Timmers, H. J. L. M., & Eisenhofer, G. (2015). Pheochromocytoma. In J. L. Jameson, L. J. De Groot, D. M. de Kretser, L. C. Giudice, A. B. Grossman, S. Melmed, … G. C. B. T.-E. A. and P. (Seventh E. Weir (Eds.), Endocrinology: Adult and Pediatric (Vol. 2–2, pp. 1902-1930.e6).
- Pohle-Krauza, R. J., Navia, J. L., Madore, E. Y. M., Nyrop, J. E., & Pelkman, C. L. (2008). Effects of l-phenylalanine on energy intake in overweight and obese women: Interactions with dietary restraint status. Appetite, 51(1), 111–119.
- Wang, Y., Chandra, R., Samsa, L. A., Gooch, B., Fee, B. E., Michael Cook, J., … Liddle, R. A. (2011). Amino acids stimulate cholecystokinin release through the Ca2+-sensing receptor. American Journal of Physiology – Gastrointestinal and Liver Physiology, 300(4), G528-37.
Entradas Relacionadas
- ¿Por qué tomar Aminoácidos Esenciales? Visita este enlace.
- ¿Es mejor tomar Proteínas o Aminoácidos? Descúbrelo aquí.




 Blog de Fitness, Nutrición, Salud y Deporte | Blog HSN En el Blog de HSNstore encontrarás tips sobre Fitness, deporte en general, nutrición y salud – HSNstore.com
Blog de Fitness, Nutrición, Salud y Deporte | Blog HSN En el Blog de HSNstore encontrarás tips sobre Fitness, deporte en general, nutrición y salud – HSNstore.com 




